國家藥監局綜合司2022年9月9日發布的《國家藥監局綜合司關于加強醫療器械生產經營分級監管工作的指導意見》(以下簡稱《指導意見》)已于2023年1月1日已正式生效。《指導意見》旨在指導各地藥品監管部門在醫療器械注冊人制度下更好地開展醫療器械生產經營監管工作。
此次涉及的醫療器械生產重點監管含39個一級類別(包含其他和未分類),涉及神經和心血管手術器械-心血管介入器械、血液凈化及腹膜透析設備、脊柱植入物等。經營重點監管包含無菌、植入材料和人工器官、體外診斷試劑、角膜接觸鏡、儀器設備等六類,涉及骨接合植入物、心血管植入物、眼科植入物等47個重點品種(類)。詳細品種目錄名單見文末。
《指導意見》要求省級藥品監督管理部門和設區的市級負責藥品監督管理的部門結合產業發展和監管實際,發揮監管資源效能,制定符合本地區實際的生產和經營分級監管細化要求,按照“風險分級、科學監管,全面覆蓋、動態調整,落實責任、提升效能”的原則,開展醫療器械生產經營分級監管工作,夯實各級藥品監管部門監管責任,建立健全科學高效的監管模式,加強醫療器械生產經營監督管理,保障人民群眾用械安全。
《指導意見》提出了對醫療器械生產經營企業的監管級別劃分原則和檢查要求,藥品監管部門可以按照風險將醫療器械企業劃分為四個監管級別,對不同監管級別的企業實施相應監管措施。對于長期以來監管信用狀況較好的企業,可以酌情下調監管級別;對于跨區域委托生產的醫療器械注冊人,僅進行受托生產的受托生產企業,以及異地增設庫房的經營企業等,應當酌情上調監管級別。對醫療器械生產企業采取非預先告知的方式進行監督檢查,對經營企業采取突擊性監督檢查。
《指導意見》要求各級藥品監管部門進一步加強統籌協調,建立健全跨區域跨層級協同監管機制;持續加強問題處置,對檢查發現的問題嚴格依照法規規章等要求及時處置;不斷加強監管能力建設,豐富監管資源,切實做好醫療器械全生命周期質量監管工作,保障人民群眾用械安全。
附件:醫療器械生產重點監管品種目錄
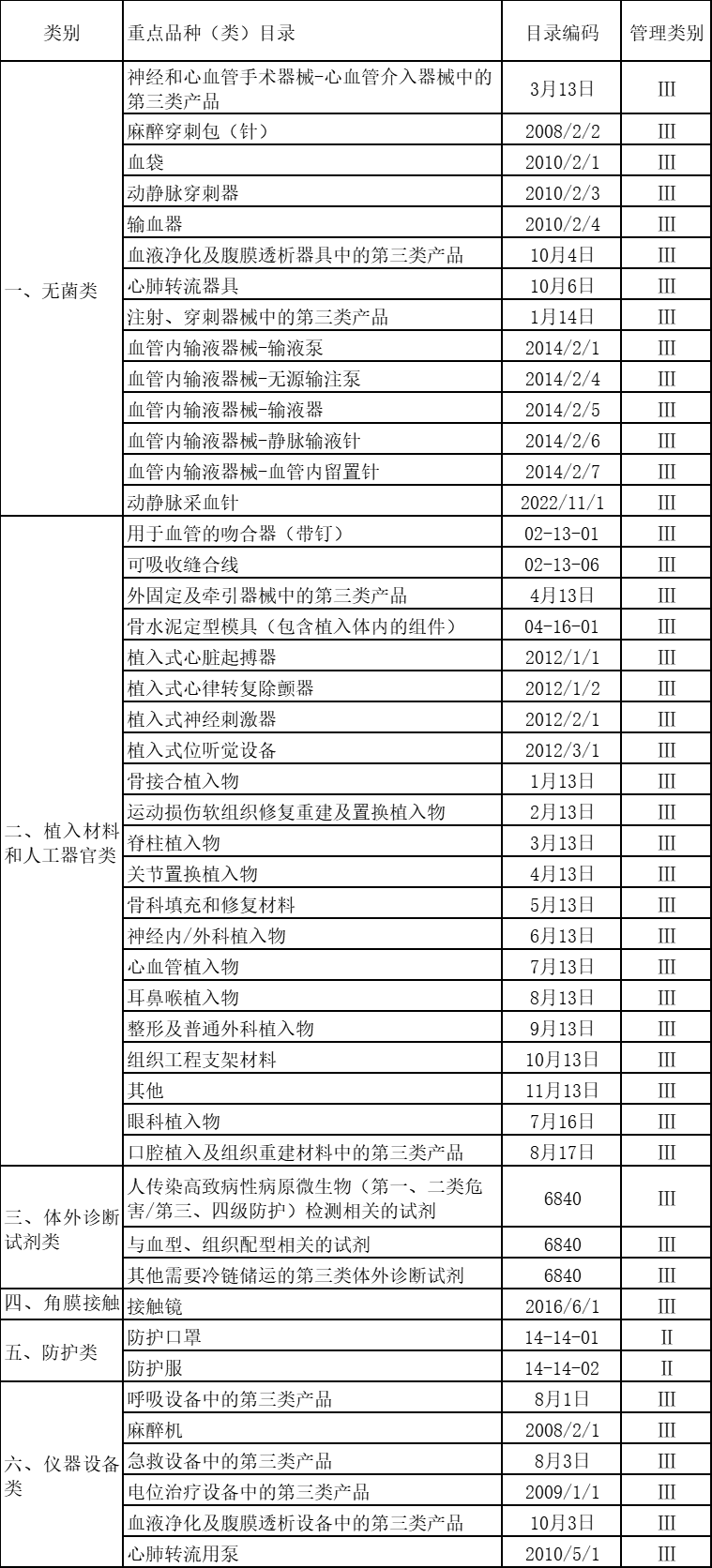
醫療器械經營重點監管品種目錄
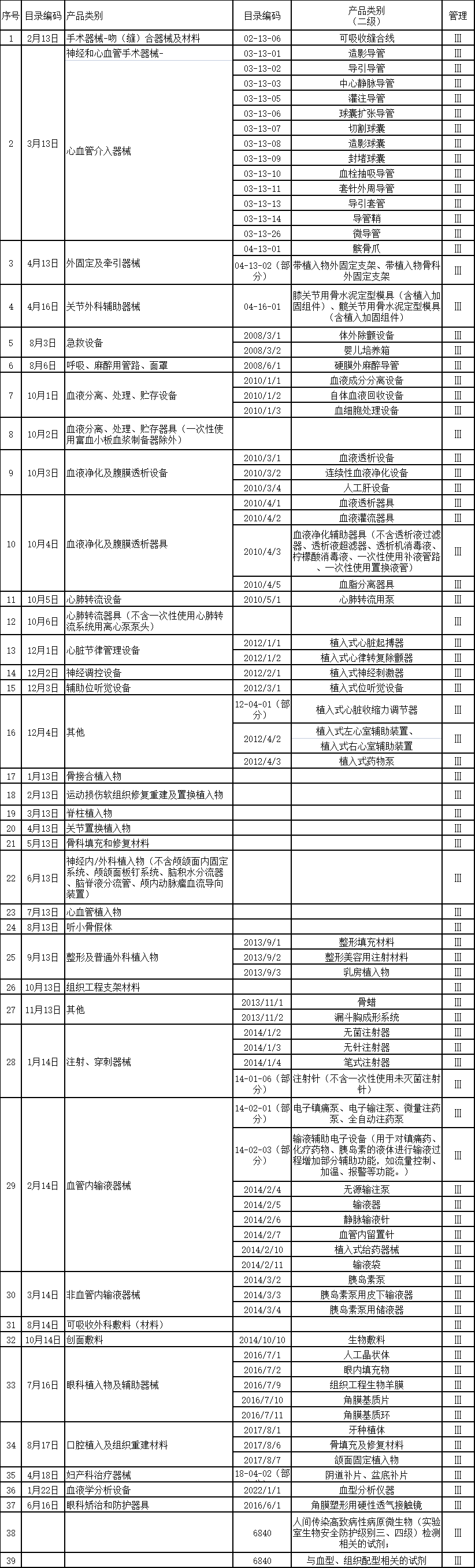




 全部商品分類
全部商品分類















