近年來,隨著醫療器械的不斷發展,醫療器械市場迎來了高提速增長,特別是2022年由于疫情的反復,使得IVD領域的獲批不斷加速。此外,境內外醫療器械在2022年獲批情況如何,一文帶你來盤點。
01 美國FDA批準情況
截至2023年1月5日,2022年FDA共批準3229個510(k)途徑的產品,其中一類器械262個,二類器械2895個,未分類72個。2022年共有22個通過上市前批準(PMA)途徑首次上市。
通過對510(k)上市前通知的器械根據美國醫學專業用途進行分類,結果發現,2022年產品獲批類型最多的為一般和整形手術器械、骨科器械、放射科器械、一般醫院和個人使用類器械與心血管器械,見圖5。

來源:美國食品藥品監督管理局 圖源:火石創造

來源:美國食品藥品監督管理局 圖源:火石創造
(二)境內批準情況
截至2022年底,2022年國家局公示了67個三類醫療器械進入創新審批綠色通道,見表2。相較于2021年的60個略有增加。

來源:國家醫療器械審評中心
表3 2014年-2022年每年進入創新審批綠色通道
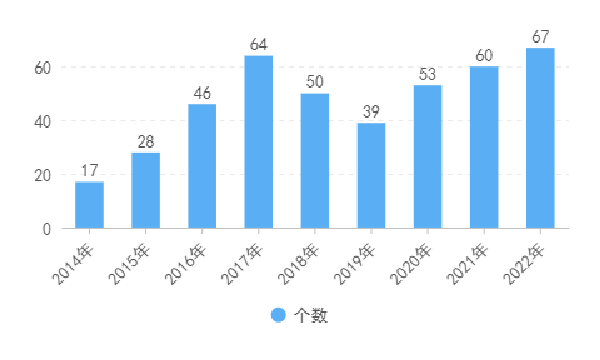
制表:醫療器械創新網
截至2023年1月5日,2022年國家局公示了54個三類創新器械獲批上市,相較2021年的35個有較大提升,見表3。截止2022年底,國家共批注188個三類創新醫療器械獲批上市,在獲批的產品當中有不少產品在全球范圍內實現了技術重大突破。例如質子治療系統、集成膜式氧合器、人工血管的獲批,也意味著國產醫療器械在多個“卡脖子”領域迎來新的突破。

來源:國家醫療器械審評中心 圖源:火石創造
表4 2014年-2022年獲批上市的三類創新器械
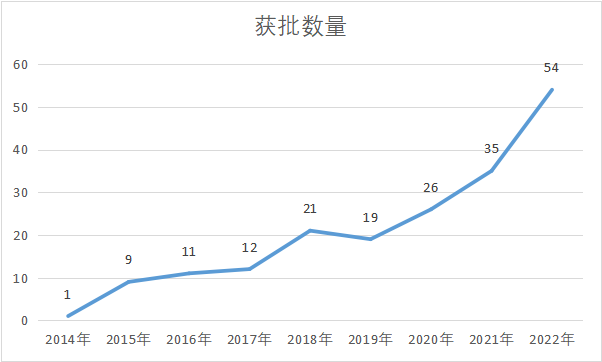
制表:醫療器械創新網
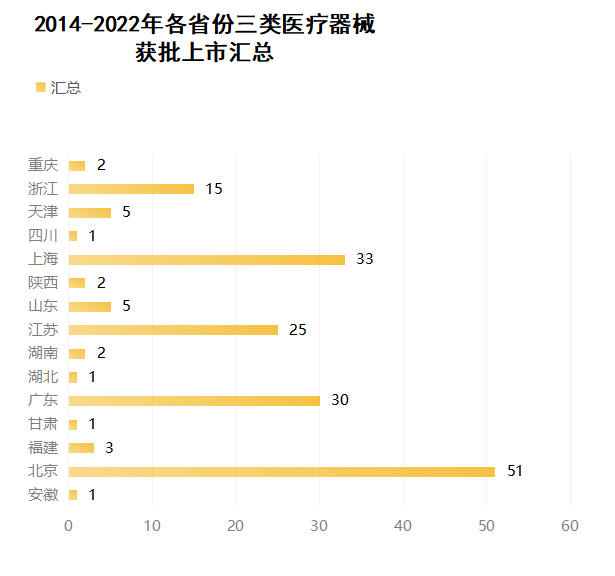
188個獲批注冊上市項目中,截止目前前五個省市分別為北京市 51項、上海市 33項、廣東 30 項、江蘇 25 項、浙江15項,五省市總和占總數的82%;
其中國產獲批177個,進口獲批11個。
截至2023年1月5日,2022年國家局共批準首次注冊三類醫療器械產品2172個,其中國產1818個,進口354個。各省級藥品監管部門2022年共批準國產第二類醫療器械注冊13063個,一類備案醫療器械27117個。
統計數據顯示,體外診斷試劑數量最多,共12628項,占29.14%,基本上均為國產,為12415項。除體外診斷試劑,批準注冊類別數量排前三位的分別為注輸、護理和防護器械,臨床檢驗器械和口腔科器械。

來源:國家醫療器械審評中心 圖源:火石創造
從地域分布上,2022年國產二、三類注冊產品批件最多的依次為廣東省(2290件)、湖南省(2277件)、江蘇省(2187件)三個區域,見圖2。

(文章來源于互聯網)




 全部商品分類
全部商品分類















