飛利浦在2021年中旬開始召回涉及數(shù)百萬臺CPAP和BiPAP呼吸機及其他呼吸設備。召回原因是這些用于治療睡眠呼吸暫停的設備中的消音組件有聲音消減泡沫,可能會降解并進入氣道。目前,飛利浦將支付至少4.79億美元,以解決召回相關的索賠。

圖片來源:飛利浦官網
在隨后的兩年中,飛利浦宣布暫時退出了呼吸設備市場,因為它正在修復這些設備。自2021年4月以來,FDA收到了105,000份問題報告 — 包括與泡沫降解問題相關的385份死亡報告。
多區(qū)訴訟聯(lián)合首席律師Levin Sedran & Berman的Sandy Duggan在與MassDevice分享的一份聲明中說:“這個無上限的和解是有史以來最大的消費者集體訴訟和解之一,隨著更多被召回飛利浦設備的用戶注冊并尋求賠償,我預計它的價值將遠遠超過預籌資金金額。”
目前,飛利浦雖然沒有對和解內容中的不當行為和過錯承認相關責任,但仍然面臨重大訴訟,要求對與召回有關的死亡、傷害和醫(yī)療費用進行賠償。具體細節(jié)還在與美國司法部進行談判。

圖片來源:飛利浦官網
與此同時,競爭對手瑞思邁在努力填補由此產生的CPAP供應鏈短缺。瑞思邁首席執(zhí)行官Mick Farrell在今年早些時候表示,世界上的一些地方的患者在被診斷出患有睡眠呼吸暫停后必須等待長達12周才能收到CPAP。Farrell說:“目前形勢比較緊張,因為仍有大量的患者需要CPAP”。他后來預測,ResMed可能會在年底之前滿足這種需求。
飛利浦召回事件的時間線 2011年至2021年4月:報告的問題很少 FDA表示,飛利浦在此期間只有30份與呼吸設備中的PE-PUR泡沫降解相關的醫(yī)療設備報告(MDRs)。只有八份報告來自美國,沒有傷害或死亡的報告。 2021年4月26日:啟動召回 飛利浦首次召回的通知,涉及特定的飛利浦雙水平正壓通氣(BiPAP)、連續(xù)正壓通氣(CPAP)和機械通氣設備,這些設備可能存在聚酯基聚氨酯(PE-PUR)聲音消減泡沫組件相關的潛在風險。 2021年6月14日:飛利浦提供更新 受影響設備的大部分在建議的五年服務壽命內都屬于第一代DreamStation產品系列。2020年的投訴率為0.03%。 飛利浦表示,經過測試,它確定PE-PUR聲音消減泡沫組件可能對用戶存在風險,包括泡沫降解成顆粒進入設備的氣道并被用戶攝取的可能性。泡沫可能會釋放某些化學物質。其降解可能會被不標準的清潔方法(如臭氧)以及高溫和高濕環(huán)境加劇。 圖片來源:飛利浦官網 2021年7月23日:FDA首次對召回進行I類指定 FDA定義為認為飛利浦設備的使用或暴露的情況下,有合理的可能性會導致嚴重的不良健康后果或死亡,因此發(fā)布了最嚴重的I類召回。 2021年7月26日:飛利浦停止接受睡眠治療系統(tǒng)的訂單 “由于優(yōu)先進行對召回設備的修復或替換行動,我們目前不接受睡眠治療系統(tǒng)的新訂單,而面罩和其他消耗品當然繼續(xù)銷售,”當時的首席執(zhí)行官Frans van Houten在財報電話會議上說。他當時表示,獲得監(jiān)管批準后需要12個月的時間來解決所有設備的問題。與此同時,飛利浦宣布暫時退出呼吸機市場。 圖片來源:前首席執(zhí)行官Frans van Houten,飛利浦官網 2021年8月:此時,美國和加拿大已經提起了一些集體訴訟 2021年8月3日:另一次嚴重的召回 FDA宣布另一次涉及飛利浦呼吸設備的嚴重召回。飛利浦在6月18日的“緊急領域安全通知”信中宣布,召回涉及數(shù)千臺V60 Plus呼吸機和所有升級為啟用高流量治療的V60呼吸機(軟件版本3.00和3.10)。如果氧氣流量因任何原因部分受阻,系統(tǒng)將發(fā)出警報后繼續(xù)為患者提供較低的氧氣流量。 圖片來源:飛利浦官網 2021年9月1日:飛利浦開始為召回的DreamStation設備進行修復和更換計劃 2021年10月8日:飛利浦在美國的多地區(qū)訴訟中,最初有10個民事訴訟 2021年11月:檢查報告稱飛利浦忽視了問題 FDA 表單483,在對飛利浦設備進行檢查后發(fā)現(xiàn),飛利浦及其泡沫供應商多年來都知道聚酯基聚氨酯(PE-PUR)聲音消減泡沫可能會分解并可能進入設備的氣道。 2022年1月:FDA將I類指定擴展到更多可能存在聲音消減泡沫問題的飛利浦呼吸設備 2022年3月:FDA命令飛利浦改進呼吸機召回的溝通 2022年4月:另一輪嚴重的呼吸機召回 FDA指定更多的飛利浦召回為I類。召回涉及飛利浦V60呼吸機的所有型號、V60 Plus呼吸機和V680呼吸機(在美國以外分發(fā))。對于這三種呼吸機的問題涉及設備內部的電路,有可能導致呼吸機停止運行。 2022年4月25日:飛利浦披露美國司法部下達了關于召回的傳票 2022年4月30日:FDA的醫(yī)療設備報告MDRs數(shù)目達到數(shù)萬 此時,FDA表示,它已經收到了超過21,000份報告聲音消減泡沫相關問題的醫(yī)療設備報告(MDRs)。該機構表示,其中126份報告提到了死亡。(FDA的醫(yī)療設備報告(MDR)系統(tǒng)是一個被動系統(tǒng),有局限性。) 2022年5月2日:FDA加強召回監(jiān)管 FDA提議一個命令,要求飛利浦提交其召回呼吸設備的計劃。 2022年6月22日:飛利浦更新召回呼吸機的測試結果 飛利浦表示,只有一小部分退回的呼吸設備顯示出聲音消減泡沫降解。 2022年7月25日:與DOJ的進行談判 在財報電話會議上,van Houten透露,美國司法部代表FDA在7月18日提供了一份擬議的同意判決。擬議的同意判決是在2021年對美國飛利浦設施進行檢查之后提出的。Van Houten表示,與DOJ的談判還處于初級階段。 2022年8月16日:FDA再次收到一批醫(yī)療設備報告 FDA表示,它已經收到了與聲音消減泡沫召回相關的69,000份醫(yī)療設備報告(MDRs),其中168份提到了死亡。 2022年9月1日:飛利浦與DOJ就回扣指控達成2480萬美元和解 美國司法部指控飛利浦誤導聯(lián)邦醫(yī)療保健計劃,向耐用醫(yī)療設備(DME)供應商支付回扣。除了2480萬美元的和解外,本周早些時候還達成了一項協(xié)議:支付420萬美元,以解決飛利浦在未經軍用適航性校正的情況下,向軍事采購商出售Intellivue MP2移動患者監(jiān)測設備的組件替代品的索賠。飛利浦仍在與聯(lián)邦檢察官就其處理呼吸設備召回的方式進行單獨談判。 圖片來源:飛利浦官網 2022年9月6日:發(fā)現(xiàn)更多問題,這次是與CPAP面罩上的磁性頭帶夾有關 飛利浦的子公司發(fā)布警告購買CPAP或BiPAP治療面罩的用戶,磁性頭帶夾或帶子可能會與植入式金屬醫(yī)療設備產生負面的相互作用。飛利浦表示,它已經分發(fā)了超過1700萬個含有磁性夾子的面罩。它收到了14份報告,暗示面罩可能已經影響了植入的設備。 2022年9月8日:飛利浦在法國面臨法律審查 路透社報道,法國檢察官已經就召回問題展開了初步調查。 2022年9月26日:飛利浦呼吸設備再次召回獲得I類標簽 新召回涉及從2020年8月6日到2021年9月1日分發(fā)的386臺呼吸機。BiPAP機器馬達中可能存在塑料,該塑料可能釋放揮發(fā)性有機化合物(VOCs)。除了用戶吸入危險的VOCs的風險外,塑料還可能導致設備故障。 2022年9月30日:飛利浦股東批準Jakobs為新CEO Roy Jakobs接替了Frans van Houten,后者已經擔任CEO超過11年。Jakobs于2010年加入飛利浦,并在多年后成為公司的Connected Care首席業(yè)務領導。他一直是公司中的關鍵人物,負責管理危機。他在2020年初主導了飛利浦對COVID-19大流行的應對。然后,他在2021年6月接手了飛利浦的召回工作。 圖片來源:飛利浦官網 2022年10月19日:FDA對飛利浦CPAP、BiPAP面罩發(fā)布I類召回 2022年10月22日:新CEO表示他對召回“深感抱歉” Jakobs表示,他們正在采取措施,使自己與其“以人為本”的意識形態(tài)重新對齊。他說:“實現(xiàn)這一點是最重要的,這需要我們加倍努力做好我們擅長的事情,繼續(xù)創(chuàng)新。修復我們讓患者和客戶失望的地方也刻不容緩。這些,也將有助于恢復我們的財務健康。” 2022年10月24日:宣布大規(guī)模裁員 飛利浦表示,它將在全球范圍內裁減約4,000個職位,占其最近年報中列出的總人數(shù)的5%。Jakobs表示,公司的首要任務是“提高執(zhí)行效率,以便我們可以開始重建患者、消費者和客戶的信任,以及股東和其他利益相關者的信任。” 2022年11月18日:飛利浦召回的呼吸設備暴露出更多問題 FDA表示,經過修復的飛利浦Trilogy呼吸機有兩個新的潛在問題。飛利浦隨后發(fā)布了一份新聞稿,稱潛在存在額外問題的Trilogy呼吸機大約占原始召回中550萬呼吸設備的3%。(這大約是165,000臺設備。) 圖片來源:飛利浦官網 2022年11月22日:飛利浦呼吸設備召回中報告了更多的死亡 FDA發(fā)布了一份更新,聲稱聲音消減泡沫相關問題的報告已增加到90,000份,其中260份提到了死亡。 2022年12月21日:飛利浦稱召回的DreamStation睡眠治療設備測試顯示 “不太可能”對健康造成傷害 飛利浦發(fā)布了召回的DreamStation睡眠治療設備相關的健康風險測試結果。測試顯示,召回設備暴露的某些排放物“不太可能對患者的健康造成明顯的傷害”。 2023年1月:非營利安全組織ECRI將家用醫(yī)療設備相關的問題,列為2023年的第一大健康技術安全問題。 飛利浦的召回事件作為案例。 2023年1月30日:飛利浦將全球員工總數(shù)再次減少6,000 Jakobs表示公司目前正在按部就班的根據(jù)計劃進行恢復,根據(jù)收益報告顯示,飛利浦將逐步恢復其在呼吸設備市場的地位。 2023年2月10日:針對飛利浦已提交的MDRs總數(shù)達到99,000。 召回已進行了一年半,飛利浦現(xiàn)在對潛在的健康風險有了更好的了解,Jakobs在更新中說。“我們非常抱歉花了這么長時間,但測試涉及長時間的調試,并且需要徹底完成。我們對于患者、醫(yī)生和客戶感到擔憂表示抱歉,我們會繼續(xù)努力滿足他們的需求。” 據(jù)FDA統(tǒng)計:針對飛利浦已提交的MDRs總數(shù)達到99,000,有346份報告提到了死亡。 第二天,Jakobs宣布任命Steve C de Baca為新創(chuàng)建的首席風險官職位。他將負責飛利浦的全球風險管理和合規(guī)性。 圖片來源:飛利浦官網 2023年3月:飛利浦與FDA達成同意判決 飛利浦同意支付1.5億美元,并同意在未來五年內進行外部審計,以解決其處理召回的方式。 2023年4月:飛利浦宣布將在未來五年內投資10億歐元,以提高其醫(yī)療設備的質量和安全性 Jakobs表示:“我們正在采取行動,以確保我們的產品和服務滿足最高的質量和安全標準。” 2023年5月:飛利浦宣布將重新進入呼吸設備市場 飛利浦表示,它計劃在2023年底之前重新進入呼吸設備市場,并在2024年初開始銷售新的呼吸設備。 2023年6月:飛利浦宣布與美國司法部達成和解 飛利浦同意支付2.5億美元,以解決與其呼吸設備召回相關的指控。 2023年7月:飛利浦宣布將在未來三年內裁減另外5,000個職位 飛利浦表示,這是為了進一步提高其運營效率。 2023年8月:飛利浦宣布將投資5億歐元,以加強其研發(fā)能力 飛利浦表示,這是為了確保其產品和服務滿足最高的質量和安全標準。 2023年9月:飛利浦宣布將在未來五年內投資15億歐元,以提高其醫(yī)療設備的質量和安全性 飛利浦表示,這是為了確保其產品和服務滿足最高的質量和安全標準。


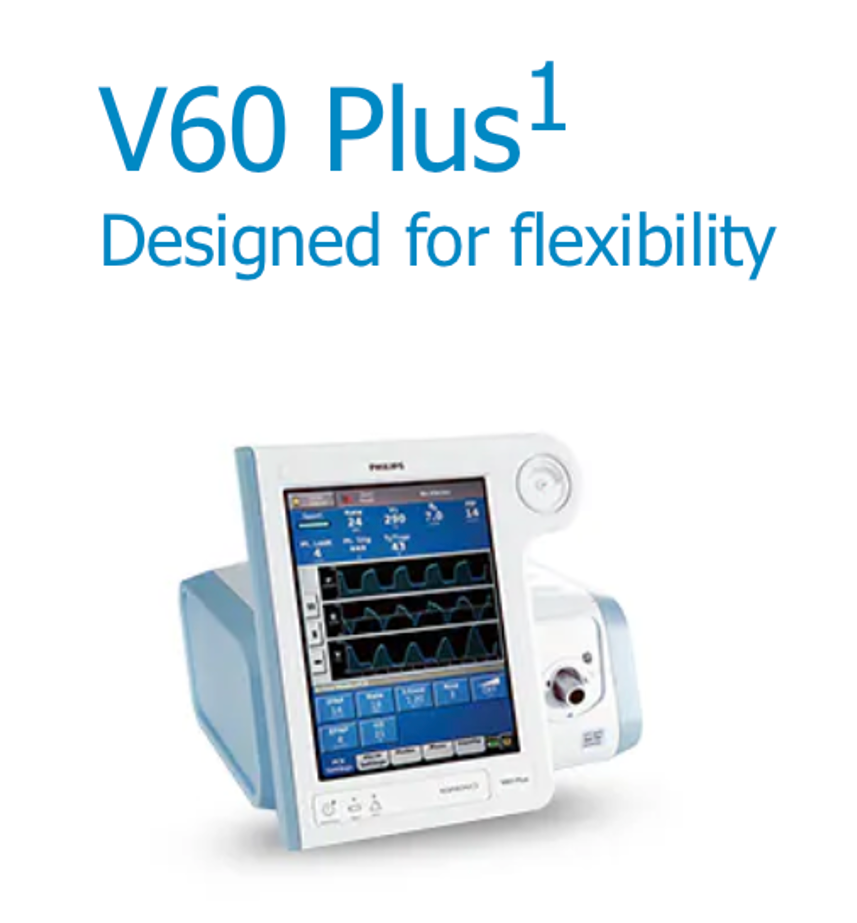



飛利浦近年來因其呼吸設備召回事件受到了廣泛關注。這一事件對飛利浦的聲譽和財務狀況造成了重大沖擊。盡管飛利浦面臨著巨大的挑戰(zhàn),但其積極的應對策略和對未來的投資承諾顯示出公司對恢復和增長的堅定信心。
(文章來源于互聯(lián)網)




 全部商品分類
全部商品分類















